
国立がん研究センター中央病院 小倉浩一先生
[Award Winner’s Story]
素晴らしい論文が認められた、学会主催アワードの受賞者たち。研究アイデアはどこから得られたのか。論文化のために、どのような工夫をしたのか。それぞれの先生に、受賞に至るまでのプロセスをインタビュー。語られる内容に、受賞のヒントが隠されているかもーー。今回はUJA論文賞を受賞された国立がん研究センター中央病院の小倉浩一先生に、論文の内容を分かりやすく解説していただきます!
登場する論文
Therapeutic Potential of NTRK3 Inhibition in Desmoplastic Small Round Cell Tumor (DSRCT)
── 自己紹介と、論文の概要を共有していただければと思います。
小倉浩一と申します。2004年に東京大学を卒業して、2006年に東大整形外科に入局し、今は国立がん研究センター中央病院で骨軟部腫瘍の臨床を専門にしています。
本日紹介させていただく論文は、Desmoplastic Small Round Cell Tumor (DSRCT)という非常に稀な軟部肉種に対する新規治療開発のもとになるような基礎研究データです。
まず私は2017年〜2020年まで、Memorial Sloan Kettering Cancer Centerという全米屈指のがんセンターに留学しておりまして、そちらでの研究成果になります。 私の留学先はDr. Marc Ladanyi labで、Marc Ladanyi先生は、最近日本でも話題なクリニカルシークエンスのMSK-IMPACTを統括する立場の方です。こちらの研究室には、非常にたくさんの方が留学していますが、MSK-IMPACTのデータを中心に、網羅的解析で発見した遺伝子以上の機能解析を主に行っている研究室です。
私は、今回の賞をいただいたDSRCTのプロジェクトの他に、ユーイング肉腫の研究をメインテーマとして行っておりました。また、最終的に研究者と整形科医のどちらにでも行けるように整形外科の臨床にも参加して、臨床見学や臨床データを使った研究もしていました。
今回紹介する論文は、アメリカにAmerican Association for Cancer Researchという学会があって、そこのオフィシャルジャーナルである、Clinical Cancer Research誌に掲載されました。
── 早速、論文の内容の共有もお願いします!
最初は、DSRCTについて紹介するところから始めたいと思います。というのも、DSRCTは非常に稀な軟部肉腫で、日本では年間2000例ぐらいの軟部肉腫の中でも非常に稀なタイプなんです。私は国立がん研究センターという非常に症例数の多い病院にいますが、それでもあまり診たことがありません。
DSRCTは主に、青年期から若年成人の男性に発症する極めて稀な軟部肉腫で、原因として非常に強力なドライバー遺伝子として、EWS−WT1融合遺伝子が同定されております。これにより異常な転写因子が生じることが、DSRCTになると考えられています。
臨床的には広範囲な腹腔内病変として発生するのが典型的で、初発時から遠隔転移を伴うことが多いことから、予後は極めて不良です。化学療法、手術、放射線治療などの集学的治療によっても、5年生存率は15%以下とされていて、有効な薬物療法の開発が急務である、まさに難治がんの代表のような腫瘍であると思っています。
次に研究結果の概要です。まず結果をまとめてしまうと、DSRCTにおいて、網羅的な発現解析によって、神経栄養因子受容体ファミリーに属する受容体型チロシンキナーゼであるNTRK3が過剰発現している。このNTRK3の過剰発現の原因は、ChIPアッセイによって融合タンパクEWS-WT1がNTRK3のpromoterに結合することであると分かりました。そして、チロシンキナーゼの恒常的な活性化によって、下流シグナルの活性化が引き起こされて、細胞増殖の亢進を誘導するということを示しました。
NTRK3の過剰発現で大変興味深いのは、それをターゲットとした分子標的治療薬があるっていうことなんです。具体的には、ROS1/TRK阻害薬entrectinibという薬があるんですが、それでNTRK3を阻害できる。この研究でNTRK3を阻害することによって、in vitro、in vivoいずれにおいてもDSRCTの増殖が抑制され治療に結びつくという成果を示すことができました。
── bench to bedsideですね。
次に厳選したフィギュアを出します。最初のフィギュアは、なぜNTRK3に注目するに至ったかを示すフィギュアです。こちらのベン図は、今回のNTRK3の同定の流れになります。
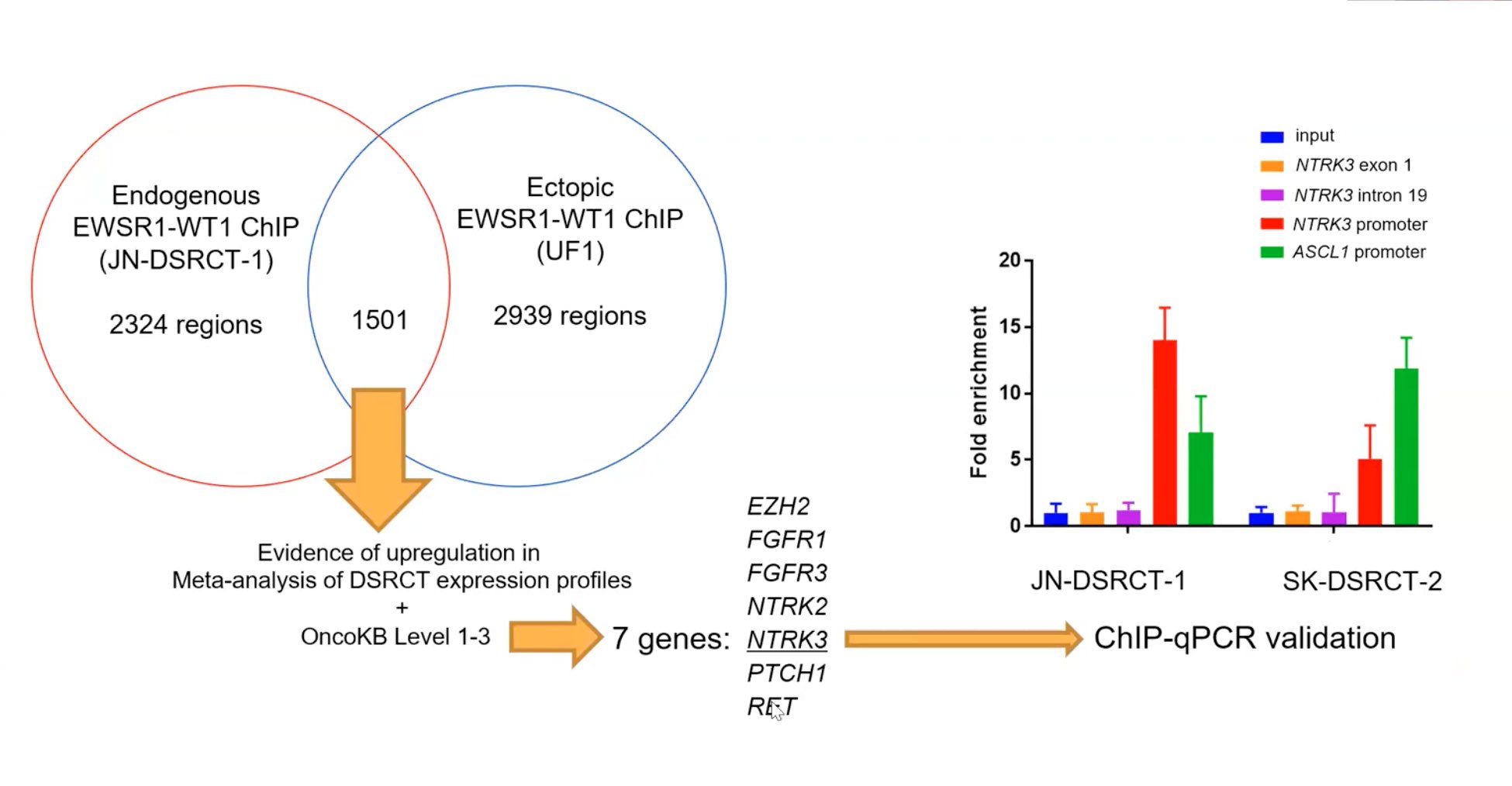
内在性にEWSR1-WT1を発言している患者由来のDSRCT細胞株であるJNと外からEWSR1-WT1をを導入した細胞株UF1に対して、WT1抗体を用いてChIPを行って、EWSR1−WT1のターゲットを探索したわけです。で、この両者をクロスリファレンスすることで、標的を見つけました。その中でたくさん標的は見つかったんですけども、特に先ほど言ったdruggableな標的として、有望な7つの遺伝子をWT1のダイレクトターゲットとして同定しました。EZH2からRETまでの7つになります。
このように網羅的解析から同定されたターゲットのバリデーションとして、ChIP-qPCRを行い、今度は2つの患者由来のDSRCT細胞株になりますが、これによってWT1がNTRK3のpromoterに結合して、WT1のダイレクトターゲットであることを示しました。
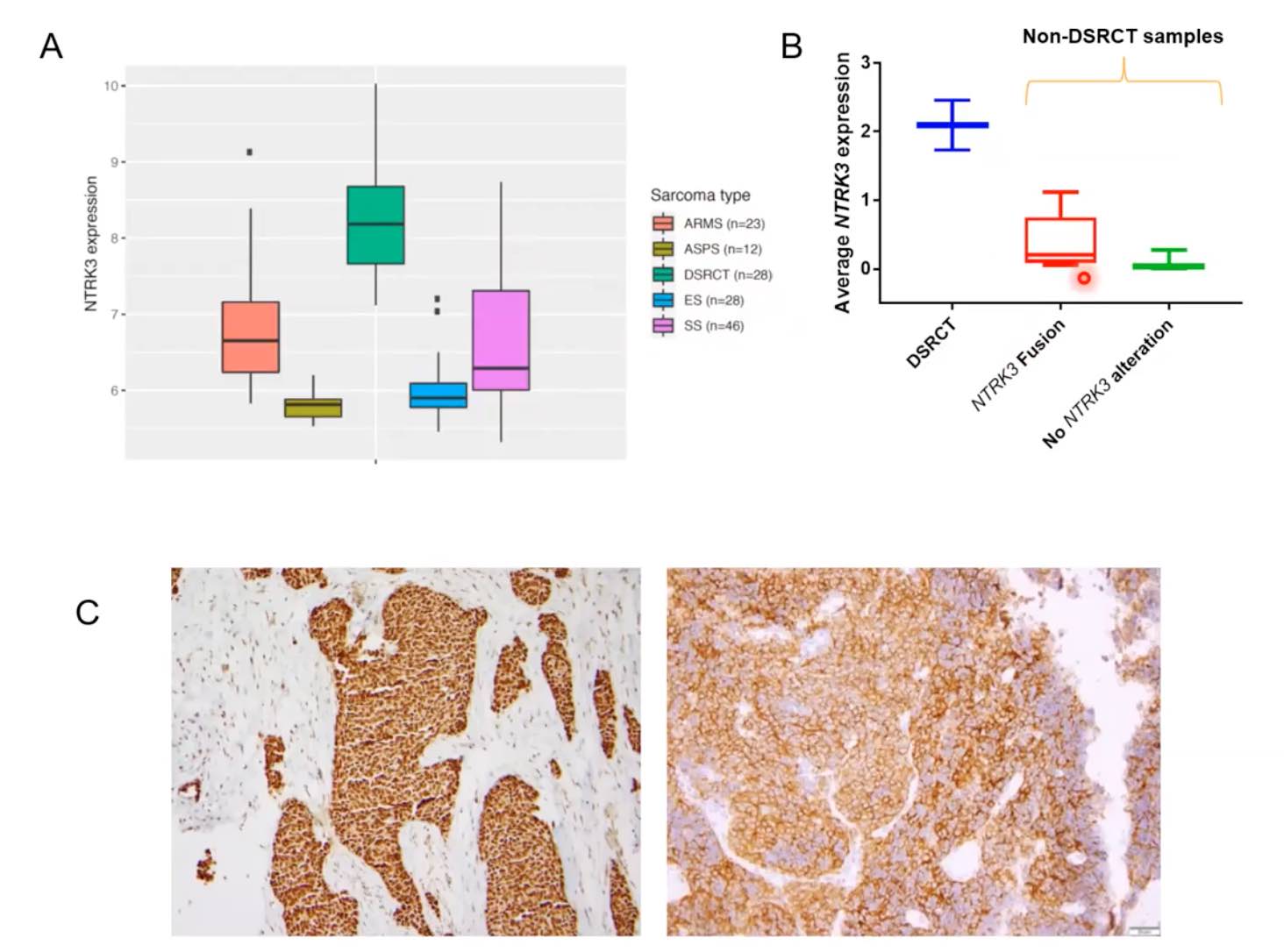
AとBがNTRK3が実際のDSRCTで高発現してることを示したフィギュアになります。いろんなアプローチで示しましたが、これはArcherっていう発現を見るようなパネルがあるんですが、そのデータです。
Aの方はちょっと略語で分かりづらいんですが、DSRCTと横紋筋肉腫、胞巣状軟部肉腫、ユーイング肉腫、滑膜肉腫などとNTRK3の発現を比べたものになります。明らかにDSRCTのNTRK3が、非常に高発現してることが分かると思います。
一方でBは、他のsarcomaではなくて、がん腫を超えてNTRK3の発現を見たものです。DSRCTとNTRK3の異常がないがん、NTRK3の融合遺伝子を持つがん、を比較したものです。融合遺伝子を持つものに比べても、明らかにNTRK3が過剰に高発現してるということが明らかになりました。
Cの方は免疫染色です。NTRK3がWT1と強く発現していると明らかになりました。
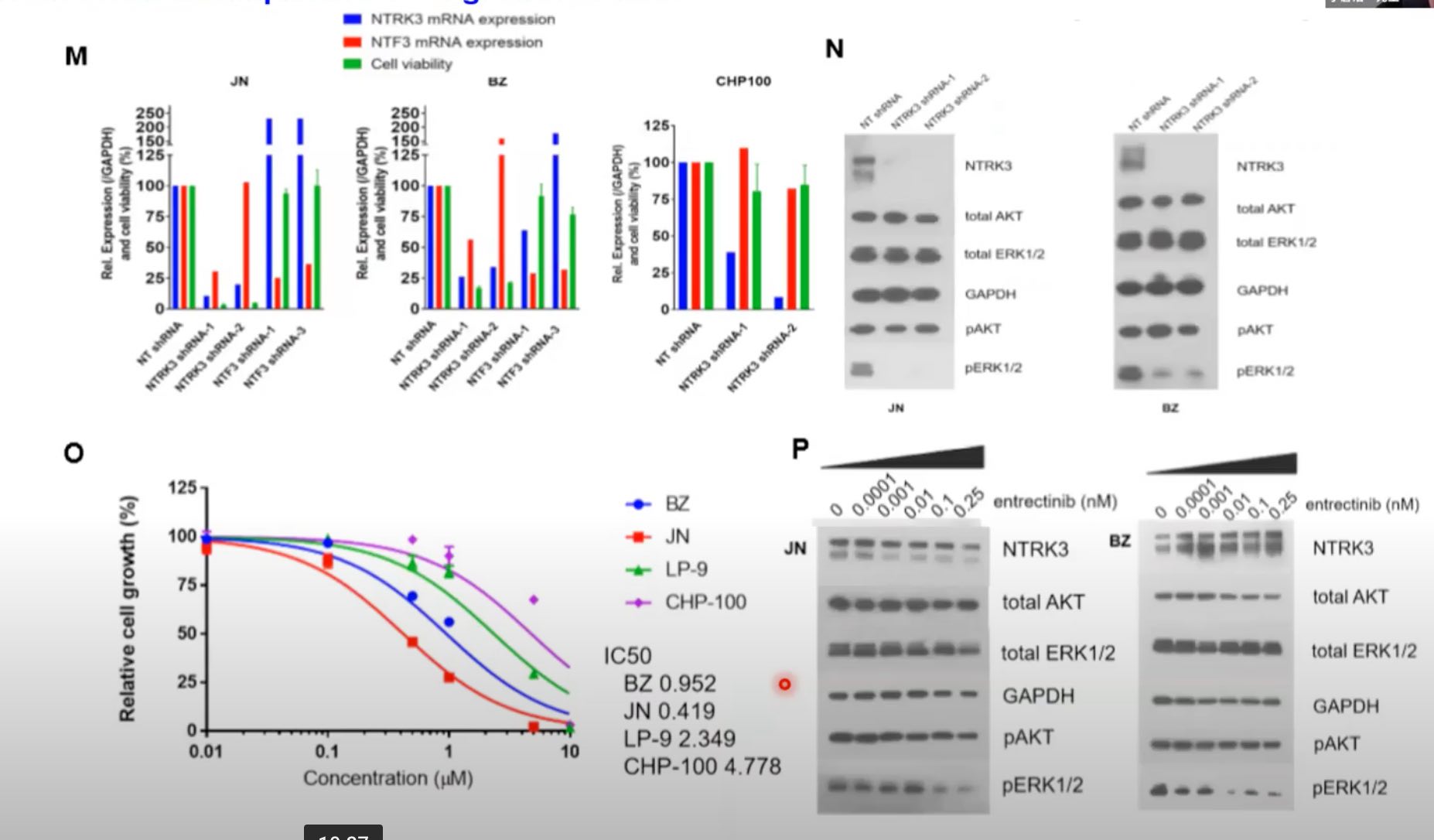
これは1番大事なフィギュアなのかなと思っているんですけど、in vitroのデータです。具体的には、NTRK3をin vitroで阻害することによってDSRCTの細胞増殖が抑制されることを示したフィギュアです。
Mのフィギュアを見ていただくと、これはshRNAでNTRK3をノックダウンした場合に何が起こるかを見たフィギュアです。緑色の棒グラフが細胞増殖ですね。JNとBZというのは、患者由来のDSRCTの細胞株で、CHP100はコントロールとして用いたユーイング肉腫の細胞株になります。DSRCTではNTRK3のノックダウンによって非常に細胞の増殖が抑えられる一方で、ユーイング肉腫では全く抑えられないという結果になって、やはりNTRK3をノックダウンすることによって、DSRCTの細胞増殖を抑える効果があるのではないかということが明らかになりました。
Nを見ていただきたいんですけども、これはNTRK3のノックダウンにより、下流の分子である ERKのリン酸が抑制されることを示したフィギュアになります。
次に、実際に薬剤でNTRK3を阻害したらどうなるかを示したのがOとPです。Oは、いわゆるIC50をBZとJNというDSRCTの細胞株と、コントロール細胞株として用いたLP-9とCHP-100を比べたものです。やはりコントロール細胞株に比べて、BZやJNではIC50が非常に低い傾向にありまして、entrectinibが細胞増殖抑制にDSRCTと働くということが示されました。
最後にPは、entrectinibをいろんな濃度で細胞に治療した時に、下流の分子のリン酸化がどうなるかを見たフィギュアです。これはやはり、用量依存的に下流のERKのリン酸化が減少することが分かりました。
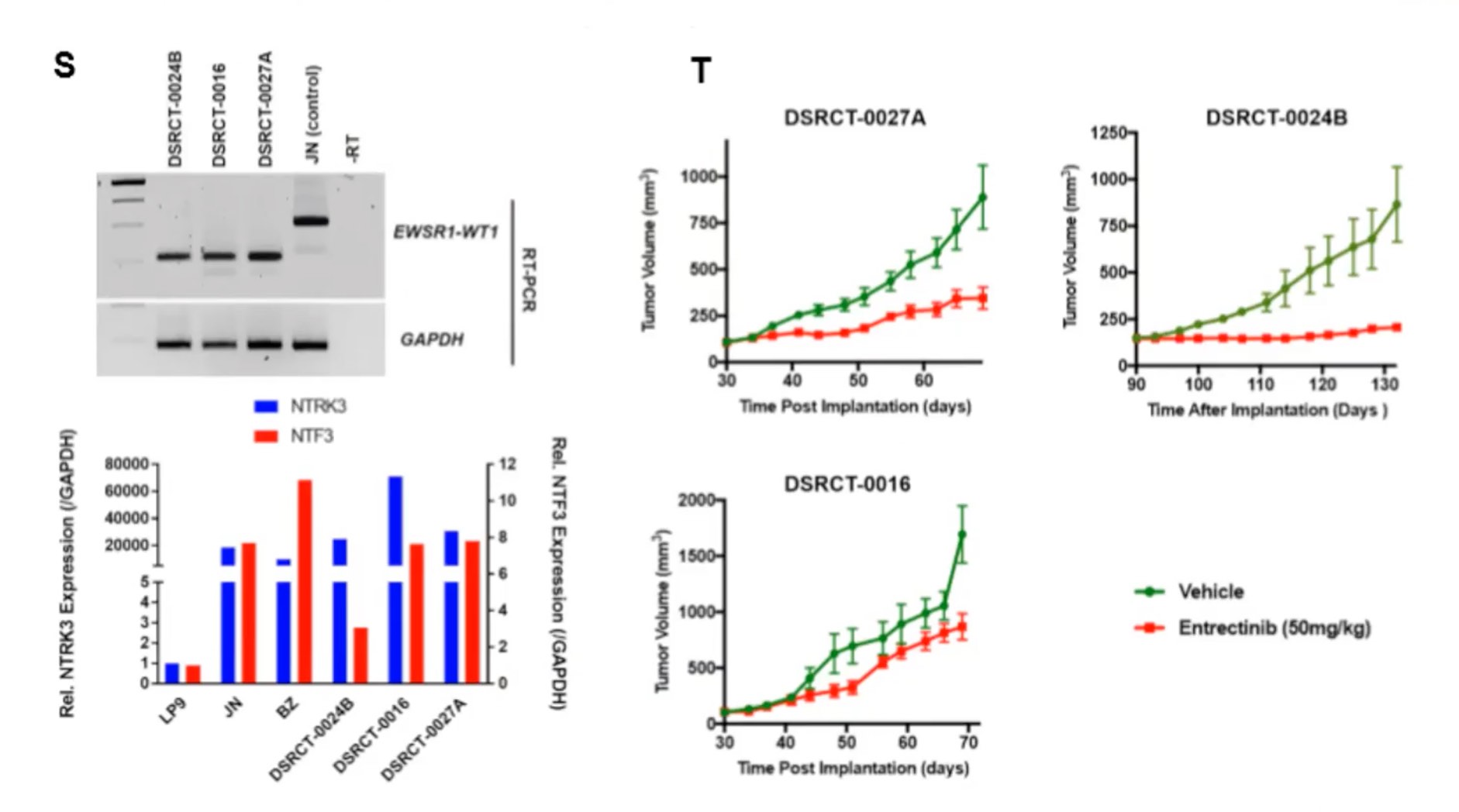
これも大事なフィギュアですね。我々の研究室でDSRCTのPDXを作製しましたが、それに対してentrectinibを使ったらどうなるか、マウスを用いたin vivo実験を示したフィギュアです。
Sに関しては、PDXモデルを作りましたよというフィギュアです。簡単に言いますと、このような3つのDSRCTのPDXモデルを作り、EWS−WT1という融合遺伝子が発現していることをRT-PCRで示しました。また、やはり作った細胞モデルでも、NTRK3が過剰発現してることを示すことができ、妥当なDSRCTのモデルであることを示しました。
最後のフィギュアTです。PDXモデルでentrectinibを投与した場合に、腫瘍の増殖が抑制されることがいずれのモデルでも分かりましたので、以上もってin vitro、in vivoいずれにおいてもentrectinibがDSRCTに有効であるということが分かりました。
結論としては、代表的な希少がんかつ難治がんであることから、DSRCTは治療開発が遅れてるのは前述の通りで、今回の研究はentrectinibがDSRCTにおいて有望な治療薬となる可能性を示したと言えると思います。実際に本研究成果を踏まえて、再発・局所進行DSRCTにおいて、NTRK阻害剤と、従来のDSRCTの治療薬であるイリノテカン、テモゾロミドを組み合わせた新規治療に関する臨床試験が、私がいたMemorial Sloan Kettering Cancer Centerで実施されることになりました。その結果を待っている段階ですが、DSRCT患者にとって、革新的な新規治療となる可能性があると考えています。
── 小倉先生ありがとうございます!ものすごく分かりやすかったです。
── どういった経緯で先生の留学は決まったんですか?
留学先をどう決めるかは、自分がこれからどういう風に医師として生きていくかの1つの岐路かなと思うんですね。例えば将来、基礎で生きていきたいなら、やっぱりがっつり基礎のできるような留学先を選ぶと思いますし。一方で私は、やっぱり臨床メインでやりたいけど、基礎もかじりたい、いわゆる米国でいうとphysician scientistとかsurgeon scientistと言うのですが、そういうキャリアを考えていました。だから臨床をしっかりやってるところを見学して選びました。
そうすると米国の2大がんセンターである、ニューヨークのMemorial Sloan Kettering Cancer CenterとヒューストンのMD Anderson Cancer Centerのどちらかかな、と。私の専門であるsarcomaの研究をしてるところは意外となくて、最後に選択肢に残ったのがMemorial Sloan Kettering Cancer Centerで、research fellowとして留学することになりました。もともと国立がん研究センターで私のボスである川井章先生が、こちらに留学した伝手もあって、紹介していただいたことが大きいかなと思ってます。
── 腫瘍領域だと、割と日本でも基礎と臨床両方に取り組んでいるイメージを持っていましたが、必ずしもそうではないんですか?
そこはなかなか難しくて、日米の研究環境の違いみたいなところまで遡らないといけないかなと思うんですけど、僕がびっくりしたのは、他のところまではちょっと分からないんですが、Memorial Sloan Kettering Cancer Centerでは基本的に、外科医でもラボを持ってるんですよ。それがすごいなと思いました。なかなか日本ではラボも運営してる外科医は少ないと思うのですけれど、アメリカではみんな持ってるんですね。少なくとも、たとえラボを持ってなくても、どこかのラボと緊密に連携して研究しています。
それで1番いいのは、コアファシリティが非常に充実していて、ほとんどの実験をやってくれるんですね。向こうでは私もその恩恵に結構預かったんですけど、余裕を持った生活をしていても、たくさんのデータを出しやすい。だからどちらかというと、研究をプランニングしたりマネジメントしたりする能力が結構重要視されているんだなと思いました。当たり前と言えば当たり前ですけど。
私の場合、日本で研究していると実験をこなすだけでいっぱいいっぱいになっちゃっていたので、コアファシリティが充実していたことには衝撃を受けましたね。そういう環境だからこそ、外科医がラボを持っても回せていけるのかなと思いました。
── その環境が作れるのは、やはり資金力があるからですか?
そこはやっぱりシステムづくりなのかな。確かにアメリカって、いろんな職種の人がいるんですよね。多民族国家だし、医療者にしたって医師の他にnurse practitioner(NP)とかphysician assistant(PA)がいるとか、すごく職種が多いじゃないですか。臨床では全部医師がやる必要はない。研究も同じようなことが言えるのかなって思ったんです。
── ゲノムシークエンスの大御所であるMarc Ladanyi先生のところにも行って、整形外科にも顔を出していたとおっしゃっていましたが、その辺りはどのようにして掛け持ちできるようにしたんですか?
昔、日本整形学会のプログラムでMemorial Sloan Kettering Cancer Centerを訪問したことがあって、整形外科の先生とも知り合いだったんです。それで「今度、病理に留学するので、整形外科の方にも行っていいですか?」とコンタクトを取り、行けることになりました。
基礎と臨床だと、動く時間帯が違うんですよ。臨床は朝が早くて、6時半からリサーチミーティングが始まったりするので、朝はそちらに参加してから、8〜9時ぐらいからラボワークを始めるっていうような感じでしたね。それは全然conflictすることなくできましたね。
あとはさっき言ったように、結構余裕をもった生活でもたくさんのデータを出しやすい環境だったので、そこまでラボに缶詰になる必要はなかったのも結構大きかったのかなと思いますね。
── 小倉先生のバイタリ的には、少し余裕がある感じだったんですね。
そうです。ラボワークの時間には臨床のことはやらないとか、ある程度のルール作りは必要かなと思いますが。臨床のことは基本的に朝と夕方以降にしていましたね。たまにラボワークの時間とかぶっちゃっていましたが、面白そうな手術があったら見に行ったりとかはしていましたけど。
でも、こういったことができるかは、ボスの性格にもよるんでしょうね。私のボスは本当に無干渉で「任せたよ」っていう感じでしたからね。
── 研究のネタは、Marc Ladanyi先生のラボ内で温められていたんですか?
おっしゃる通りで、私はユーイング肉腫の研究がメインでした。このDSRCTのプロジェクトは前任者か前々任者かが途中までやってスタックしてたのを見つけたんです。「面白そうなのに、なんで手をつけないんだろう?」と思って、ボスにちょっとこれやってもいいですかと言ってみたら「ぜひやってくれ、やる人いなくて困ってたんだ」と返ってきたので始めました。
自分でゼロから始めるのも大事かもしれないけども、前任者がある程度道筋をつけてくれたものを引き継いでやるのもいいなと思っています。
── NTRKに阻害薬があるというのは、既知のことだったんですか?
NTRKって、肺がんや肉腫もそうなんですけど、融合遺伝子があってentrectinibはめちゃくちゃ効くんですよ。融合遺伝子を持つ肺がんが消えちゃうぐらい効くので、これはいい標的だと思って取り組みました。
── 最後の結論のスライドでも言ってくださったように、既存の薬と組み合わせた新規治療に関する臨床試験が行われる流れになってるのは、凄く良いニュースですよね。
やっぱり研究者としても医師としても、こういう風になってくれるのは本当に研究者冥利に尽きるというか、嬉しいなと思います。
── 論文が実際にpublicationされた後にこういう話になったんですか?それとも同時並行で進めていたんですか?
同時並行でほぼやってるんですよ。小児科の先生とはよくコミュニケーションを取っていて「こういうのをやりたいんだ」っていうのは、もともと話として聞いていましたし。
すごいなって思ったのは、このスピード感。この研究でこういう成果が出てた、では臨床試験やろう、という。あまり日本にはないかなと思いました。
あとは、Memorial Sloan Kettering Cancer Center小児外科の先生で、DSRCTの手術をしまくっている先生がいらっしゃったんです。それでPDXも、あれだけたくさん作ることができたのは、すごい大きいと思いますね。
これまでのがん研究におけるゼノグラフトモデルは、いわゆる細胞株をマウスに移植していたんですけど、細胞株を移植したモデルの信頼性が低いんですよ。患者さんのを移植したモデルの方が、やっぱり信頼性は高い。ただ、PDXを作るのにコストがすごくかかるし、時間もかかる。そもそも患者さんの細胞由来のものですから、患者さんがいなければできません。希少な肉腫とかも含めて非常に充実していて、バンクがある研究環境はなかなかないので、すごい環境だなと思います。
── publication後の反応としては、日本の先生からもありましたか?
がんセンターで働いている内科や小児科の先生方は論文読まれていて、すごいと言っていただきました。この論文もそうですし、ユーイング肉腫の方の論文も出た瞬間に「先生、載っていたね」と言っていただきますね。
── ユーイング肉腫関連や、より整形外科寄りの論文も留学中に何本も出されていたと思うのですけれど、整形外科にも顔を出していたから、そこのデータも触らしてもらえるような関係性だったんですか?
そうですね。
── 顔を出すぐらいはできる気もしますが、ちゃんとデータをもらって論文にしてしまうのがすごいですね。最初のデータをもらう入口と、最後までやり切ってpublicationする出口までたどり着くコツはなんでしょう?
自分がそんな優れてるとは全く思わないんですけど、たぶん最初に行ってカンファとかに参加していると、ちょっとやっぱり居心地が悪いじゃないですか。言葉の問題もあるし、あとはclinical fellowとresearch fellowの立場の違いとかもあるので、やっぱり最初の3カ月ぐらいで辛くなってくるんですよ。
日本人の留学生とかもたまに臨床にも来るんですけど、最初のうちは顔を出しているんだけど、カンファの内容は日本と変わらないので「日本に帰ってからやればいいか」という感じで、挫折していく人も見てきました。でも、そこを我慢することですよね。聞き取れないこともあって恥ずかしい思いもするけど、そこを我慢して、仲間になるというか、そういうところがコツかなと思いますね。
── 顔を出しているだけの整形外科では、どうやって信頼を勝ち得ていくんですか?
それはやっぱり整形外科のボスとも定期的にアポを取って面談するようにしたことですね。「こんなことを考えているんだけど、こんなことやっていいですか?」とか面談で伝えて、データを集めて「ここまでこういうデータが出ているんですけど、これで論文書いていいですか?」とか。だから、途中で結構挫折しそうになるので、月1回ミーティングするぞって決めて努力していくことかなと思います。
「こいつ、言葉もあんまり上手くないし」とか思われると思うんですけど、そうやってしつこく食い下がってると、そこを評価してくれるのかなとは思いました。そうしていかないと、多分続かない。
── 定例ミーティングはいいですね。そうすれば、言葉はあんまり上手くなくてもパッションは伝わりますよね。小倉先生は留学中に、たくさんの良い論文を出されているので、興味を持った方はぜひチェックしてみてください。ものすごい仕事量と質だと感じてもらえると思います。ありがとうございました!